

Nuevos fármacos, ¿nuevas oportunidades? Anticuerpos monoclonales – guiaterapeutica. La señora Concepción tiene 34 años y acude a la consulta por un cuadro de estreñimiento que relaciona con el inicio de una nueva medicación para la migraña, erenumab (Aimovig®), que le han prescrito en el hospital y lleva tomándolo desde hace cinco semanas.

Presenta migraña desde los 22 años. Describe las crisis como cefalea que se localiza en la zona supra y retroorbitaria y que cede con su medicación sintomática habitual (AINE o triptanes). La frecuencia de las crisis era de unos 8-10 episodios al mes. Desde hace 2-3 años ha aumentado la frecuencia de las crisis hasta presentar unas 18-20 crisis al mes. Para su profilaxis, en estos dos años, ha sido tratada primero con propranolol y luego con topiramato, sin que disminuyera la frecuencia de los episodios de cefaleas. ¿Qué es el erenumab?
Biosimilar Ther Initiative. CDER List of Licensed Biological Products 1 21 2020. Biosimilars. Congress, through the Biologics Price Competition and Innovation Act (BPCI Act) of 2009, created an abbreviated licensure pathway for biological products that are demonstrated to be biosimilar to or interchangeable with an FDA-approved biological product.
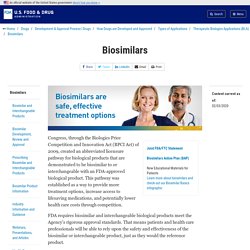
This pathway was established as a way to provide more treatment options, increase access to lifesaving medications, and potentially lower health care costs through competition. FDA requires biosimilar and interchangeable biological products meet the Agency’s rigorous approval standards. That means patients and health care professionals will be able to rely upon the safety and effectiveness of the biosimilar or interchangeable product, just as they would the reference product. Visit the pages below to learn more: Hoja informacion pacientes Biosimilares SERMAS 2019. ABCD Position Statement Insulina BS. Biosimilares grupo psoriasis. ESNO position statement on biosimilar medicines.
Biosimilar nurses guideline final. PosicionamientoSEHH biosimilares. PosicionamientoBiosimilaresSEFH documentocompleto Definitivo. POSICIONAMIENTO SER 2018. Eahp position paper biosimilar medicines june 2018. GUIA BIOSIMILARES FARMACEUTICOS. IQVIA Biosimilar 2018 V7. La Regulacion y financiacion de los biosimilares en la OCDE weber (1) Intercambiabilidad biosimilares SEFarmacología.
Percepción y actitud. Advancing Biosimilar Sustainability in Europe - IQVIA. About the Report A growing number of biologic medicines have been developed and approved over the past decade, improving the lives of patients worldwide.
However, patient access to biologics has been limited, partly due to their relatively high cost. Biosimilars are increasingly available across Europe, bringing with them the opportunity to generate competition for biologic therapies and thereby lower medicine costs and increase patient access. This report puts forth a framework for the evaluation of sustainability in the biosimilars market and identifies its key policy elements. Based on these criteria, current policies and market dynamics are assessed to identify where risks to sustainability exist and the best practices that can support the long-term positive contribution of biosimilars in Europe.
Report Summary Biosimilars are now an integral part of the market for biologics, which accounted for $277 billion in sales globally in 2017 and is projected to reach $452 billion by 2022. La penetración de los biosimilares está en el 3% del mercado hospitalario. Los FH destacan su papel en adherencia y apoyan la decisión colegiada para el uso de biosimilares. La Sociedad Española de Farmacia Hospitalaria (SEFH) ha organizado una jornada, en colaboración con la Escuela Andaluza de Salud Pública (EASP) y con el apoyo de Laboratorios Gebro Pharma, sobre enfermedades autoinmunes, titulada ‘Visión Multidisciplinar.

Mejoras de Resultados en Salud’, en la que, según la SEFH, han tenido lugar varios debates constructivos en búsqueda de la generación de futuros grupos de trabajo multidisciplinares para abordar la necesidad de incorporar objetivos de resultados en salud, protocolos, y herramientas útiles de cara a evaluar de forma continua la manera de tratar estas patologías. Durante su intervención, la directora de la EASP, Reyes Álvarez-Ossorio, ha destacado la importancia de la "colaboración con la SEFH y la necesidad de establecer un trabajo coordinado ante la complejidad de estas enfermedades, para mejorar los resultados en salud".
Once nuevos biosimilares aprobados ya en España, a la espera de llegar al mercado - Diariomedico.com. De los 31 biosimilares autorizados en España, once están pendientes de lanzamiento, según datos de la Asociación Española de Biosimilares (Biosim).
Entre éstos hay dos que aspiran a arañar ventas a Humira, de Abbvie, que lleva años encabezando el ranking mundial de medicamentos en ingresos. Son los adalimumab biosimilares de Amgen y Samsung Bioepis. La primera también espera a corto plazo poder competir con el superventas Herceptin, de Roche, con su trastuzumab biosimilar. Entre los medicamentos de uso hospitalario, se espera que aumente la competencia en el segmento de filgastrim, con el lanzamiento de un biosimilar de Ratiopharm y otro de Teva, que se suman a los ya comercializados de Sandoz, Hospira y Accord.
Clínicos piden más evidencia para intercambiar originales por biosimilares. Las sociedades científicas, a nivel general, coinciden en la gran aportación que pueden realizar los biosimilares a la sostenibilidad del sistema de salud.

Incluso algún especialista reconoce los avances de algunos de ellos en lo que respecta a facilitar la vía de administración o la biodisponibilidad. Tampoco faltan las voces clínicas que destacan la aparición del biosimilar como palanca para la generación de futuras innovaciones. Pero dicho esto, y pese a que todos muestran su confianza en el rigor de la Agencia Europea de Medicamentos (EMA) cuando aprueba un medicamento, citan las incertidumbres asociadas a posibles efectos adversos o pérdidas de eficacia al intercambiar el original por el biosimilar, así como los requisitos (parece ser que insuficientes, a juicio de los especialistas) que se exigen para la extrapolación de indicaciones, para explicar la penetración aún baja de estos productos.
Prescriptores, industria y juristas coinciden: no se puede sustituir un medicamento sin contar con el médico. SEFH: El concepto de ‘sustitución’ de biosimilares no es aplicable al hospital. La Sociedad Española de Farmacia Hospitalaria (SEFH) considera que en “un sistema participativo y explícito de selección de medicamentos” como el que se produce en las Comisiones de Farmacia y Terapéutica de los hospitales, “el concepto de ‘sustitución’ no es aplicable al ámbito hospitalario, en el que es el proceso de “selección” consensuada de los medicamentos el que toma de decisión de los medicamentos disponibles en el hospital, a diferencia del ámbito de Atención Primaria”.

Según el escrito de los farmacéuticos hospitalarios, la calificación de ‘no sustituibles’ que tienen los medicamentos biológicos, no es de aplicación al hospital. En cualquier caso, los farmacéuticos hospitalarios rechazan que la selección de medicamentos realizada en los hospitales implique “una restricción o confrontación con la aludida libertad de prescripción”, sino que, según indican, se trata de “una garantía de que se realiza en base a criterios científicos de beneficio-riesgo y de coste-efectividad”.
Los reumatólogos dicen ‘no’ a la sustitución por biosimilares en SFH. Posicionamiento Biosimilares SEFH VF. Las nueve claves de la SEFH en relación al manejo de los biosimilares. Evolución del mercado de medicamentos biológicos con y sin competencia de medicamentos biosimilares. Guia medicamentos biosimilares. Austr Prescr 2016 biosimilars 39 188. WeMerecBiosimilars. EMA Guía informativa para profesionales sanitarios. INFAC Vol 24 n 3 biosimilares. Vistazo I glargina con precio modificado. Boletín 12 Octubre. biosimilares y paracetamol junio 16. Nº 36 Medicamentos biosimilares despejando dudas[1]
Martos Rosa Farm Hosp 2015 Biosimilares. Guideline on biosimilar EMA. Decalogo del medicamento biosimilar. Ojo de Markov 69 Medicamentos Biosimilares a qué esperamos.