Feux d'artifice. Avec la découverte en Chine plusieurs siècles avant JC de la combustion de la matière organique accélérée par le salpêtre (nitrate de potassium) et l’invention de la poudre (également connue sous le nom de la poudre noire) vers 220 avant JC, l’Humanité a une fascination pour les feux d’artifice qui ne cessera probablement jamais.
Aujourd’hui, les applications techniques qu’offre la pyrotechnie en plus des feux d’artifice, tels les airbags (cf. Azoture de sodium), des extincteurs, les fusées d’alarme, les allumettes, la production de mousses nanoporeuses et de propulseurs sont de plus en plus nombreuses. Le développement et la recherche en ce domaine sont toujours d’actualité avec notamment l’extension aux matériaux énergétiques. Les feux d’artifice furent inventés en Chine au VIIe siècle pour éloigner les esprits maléfiques. Les chlorates libèrent autant d’oxygène qu’ils en contiennent :2 ClO3- ------ 2 Cl- + 3 O2 Sources. Les principes des feux d'artifice.
Pour comprendre les principes des feux d’artifice il faut tout d’abord avoir quelques notions de chimie.
Elles sont dans l’ensemble simples à comprendre, leur mise en œuvre en revanche devient plus compliquée. 1 L'oxydo-réduction C’est à cette catégorie de réaction qu’appartiennent les réactions d’explosions et de combustions et donc les réactions pyrotechniques. Le terme comporte deux mots : oxydation et réduction. Ces deux phénomènes se produisent simultanément lors d’une réaction d’oxydo-réduction. Pour écrire cette réaction et déterminer s’il y aura ou non une oxydo - réduction, il faut déterminer les demi-équations de la réaction, ce qui consiste à faire apparaitre clairement le transfert d’électron. Principe de combustion et de propulsion - Les feux d'artifices. Oxyde. Un article de Wikipédia, l'encyclopédie libre.
Un oxyde est un composé de l'oxygène avec un élément moins électronégatif, c'est-à-dire tous sauf le fluor. Oxyde désigne également l'ion oxyde O2-. Description[modifier | modifier le code] De manière générale, on définit un oxyde comme un composé chimique constitué d'oxygène avec un autre élément chimique moins électronégatif. Selon le composé associé à l'oxygène et son degré d'oxydation, l'oxyde est moléculaire (eau, dioxyde de carbone) ou cristallin avec une structure qui va d'une forte ionicité (Na2O, CaO) à des solides semiconducteurs (FeO).
Les oxydes ont une structure, en général, cristalline, bien que certains soit amorphes (comme le verre, forme amorphe de la silice). 3 - Les couleurs - TPE sur les feux d'artifice. Nous nous intéressons à la flamme issue de la combustion de la poudre.

Cette flamme, comme tous les matériaux qui nous entourent est constituée d'atomes. Les électrons de l’atome se trouvent sur une couche, en principe ils ne se soucient pas des autres couches mais sous l'effet de la chaleur, certains électrons captent l'énergie thermique. A cause de cette énergie, ils ne peuvent rester sur leur couche initiale et se déplacent sur la couche supérieure.
Pour redescendre sur leur couche initiale, ils doivent perdre l'énergie qu'ils ont acquise, sous forme thermique et en libérer sous forme lumineuse : quand un électron retourne sur sa couche, il restitue un photon : une particule élémentaire qui constitue la lumière. Les couleurs des feux d'artifice. Les premiers feux d’artifice ne possédaient que deux couleurs : l’or (jaune orangé) et l’argent (blanc), car les connaissances chimiques de l’époque ne permettaient pas d’en créer d’autres.
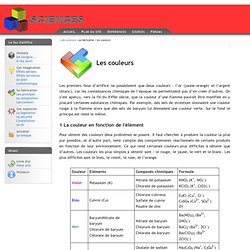
On s’est aperçu, vers la fin du XVIIIe siècle, que la couleur d’une flamme pouvait être modifiée en y plaçant certaines substances chimiques. Par exemple, des sels de strontium donnaient une couleur rouge à la flamme alors que des sels de baryum lui donnaient une couleur verte. Sur le fond le principe est resté le même. 1 La couleur en fonction de l'élément Pour obtenir des couleurs deux problèmes se posent. 2 Le digramme de chromaticité CIE La nature tridimensionnelle des couleurs (4 couleurs sont toujours reliées linéairement par cC=rR+vV+bB) suggére de porter la valeur des trois composantes des trois couleurs primaires sur trois axes orthogonaux.
Carrefour atomique - Feux d'artifice. La chimie pour le plaisir des sens!

Certains prétendent que la roue est la plus grande invention de toute l'histoire tandis que d'autres diront que c'est le feu qui a changé le plus notre façon de vivre. Un fait est certain, c'est que le feu a été exploité sous presque toutes ses formes et il le restera encore pour longtemps. Il a été utilisé pour sa chaleur, sa lumière, sa destruction, et maintenant, on peut même l'utiliser pour se divertir grâce à l'invention des feux d'artifice. Feux d'artifices. La Propulsion ..........

Les Effets .......... La Lumière Retour au début de la page. Aspects chimiques : C'est probablement avec les premières armes à feux qu'est apparue la poudre noire ou poudre à canon; il fallait une matière susceptible de brûler rapidement et en même temps produire un volume important de gaz. Ainsi, en trouve-t-on les traces chez les Chinois qui, d'après l'Allemand VON BOMOCKI, utilisaient des flèches incendiaires propulsées par un mélange semblable à la poudre à canon au XIe siècle. Au XIVe et XVe siècle, la composition était (en masses): 6 parties de salpêtre pour une partie de soufre et une partie de charbon de bois. 30 % de charbon, 30 % de soufre, 40 % de salpêtre pour la poudre de mine (lente), ou bien 12 % de charbon, 10 % de soufre, 78 % de salpêtre pour la poudre de chasse, ou encore 12,5 % de charbon, 12,5 % de souffre, 75 % de salpêtre pour la poudre dite de guerre.
Les dangers et les réglementations françaises - Les feux d'artifices. Feu d'artifice. Un article de Wikipédia, l'encyclopédie libre.