

Enquête de santé (France 5) : quand le médicament tue au lieu de soigner. En France, 18.000 décès et 150.000 hospitalisations seraient liés chaque année à une erreur médicamenteuse.
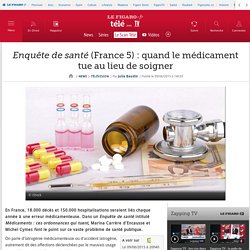
Dans un Enquête de santé intitulé Médicaments : ces ordonnances qui tuent, Marina Carrère d'Encausse et Michel Cymes font le point sur ce vaste problème de santé publique. On parle d'iatrogénie médicamenteuse ou d'accident iatrogène, autrement dit des affections déclenchées par le mauvais usage des médicaments, de l'interaction à la surdose en passant par l'effet secondaire inattendu, l'automédication ou la mauvaise prescription. Et ce sont les personnes âgées qui paient le plus lourd tribut. Selon la Haute Autorité de santé (HAS), en effet, les accidents iatrogènes sont deux fois plus fréquents après 65 ans, certains avec des conséquences graves, et, dans 20 % des cas, conduisent les octogénaires à une hospitalisation. Un problème de santé publique d'autant plus préoccupant que ces incidents pourraient, pour la plupart, être évités. Restent bien sûr le b.a.
Des médicaments «plus dangereux qu’utiles» Des médicaments prescrits à coups de millions de dollars au Québec devraient être retirés du marché parce qu’ils sont «plus dangereux qu’utiles», estime une prestigieuse revue française.
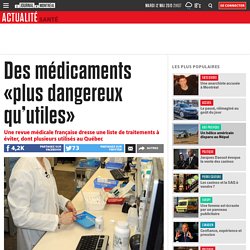
Pour la troisième année de suite, la revue Prescrire a publié récemment sa liste de médicaments à éviter «pour mieux soigner». Troubles neurologiques, problèmes cardiaques, dépression, réactions allergiques graves: les effets secondaires associés à ces traitements sont multiples, insiste l’étude. «Il n’y a pas de situation où le jeu en vaut la chandelle, où ils sont plus utiles que dangereux, a indiqué au Journal Bruno Toussaint, directeur éditorial de Prescrire. Tous les médicaments ont une certaine efficacité et un danger. 6 médicaments dangereux délivrés sur ordonnance. Vous pouvez faire confiance à votre médecin, mais prenez conscience de tous les médicaments qu’il vous prescrit et assurez-vous qu’ils ne sont pas dangereux pour vous.
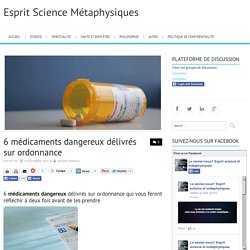
Les dernières études ont montré que la plupart des médicaments populaires délivrés sur ordonnance ont des effets secondaires potentiellement graves, allant des nausées à court terme et des maux de tête à la myopathie et aux maladies cardiaques de nature inflammatoire – et encore pire dans certains cas. Beaucoup de gens ne sont pas au courant de ces informations importantes, et croient encore au ‘mythe’ que les avantages des médicaments approuvés par la FDA ou l’ANSM l’emportent largement sur les risques éventuels. Afin de mettre les choses au clair, cet article couvre six classes de médicaments délivrés sur ordonnance qui ne sont pas tout à fait sûrs pour la santé. 6 médicaments dangereux: 1. 2.
Thanks! - TEXF-PF-2002-00120024-2.PDF. Décongestionnants ORL : à retirer du marché, au lieu de les dérembourser'', 1er avril 2012. Les décongestionnants vasoconstricteurs utilisés par voie orale ou nasale dans les rhumes, les rhinites allergiques, les rhinopharyngites ou les sinusites, exposent à de nombreux effets indésirables, dont des troubles cardiovasculaires parfois mortels.

Fin 2011 et début 2012, la Commission de la transparence a réévalué ces médicaments et a considéré que leur service médical rendu est insuffisant, mais uniquement en cas d'association avec un corticoïde, un anti-inflammatoire non stéroïdien, un antiseptique ou un mucolytique. Il s’agit de : Dérinox° (naphazoline + prednisolone), Déturgylone° (oxymétazoline + prednisolone), Rhinadvil° et Rhinureflex° (pseudoéphédrine + ibuprofène), Rhinamide° (éphédrine + acide benzoïque) et Rhinofluimucil° (tuaminoheptane + acétylcystéine + chlorure de benzalkonium). La Commission a recommandé leur déremboursement. ©Prescrire 1er avril 2012. Untitled. Dépendance aux médicaments pharmacodépendance. Médicament sous "surveillance supplémentaire" : un triangle noir sur les notices'', 1er novembre 2013.
La réglementation prévoit une surveillance des effets indésirables des médicaments, dénommée pharmacovigilance.
Celle-ci est primordiale, car les effets indésirables, notamment ceux peu fréquents ou survenant après une utilisation prolongée, ne sont pas ou peu connus au moment de l'autorisation de mise sur le marché (AMM) d'un médicament. Dans certains cas, les autorités de santé organisent une surveillance présentée comme plus active, par exemple : en cas de substance nouvelle ou d'AMM dérogatoire, c'est-à-dire octroyée sur des données partielles à compléter après la commercialisation.
Cette surveillance est qualifiée dans la réglementation de "surveillance supplémentaire". La transposition en droit français de cette réglementation impose l'apparition du triangle avant fin 2013 en France. D'une manière générale, le triangle noir signale un manque de connaissance sur le médicament. ©Prescrire 1er novembre 2013. Dompéridone (Motilium° ou autre) et troubles cardiaques : à écarter sans attendre'', 1er septembre 2013.
La dompéridone (Motilium° ou autre) est un neuroleptique commercialisé notamment dans les troubles digestifs comme les nausées et les vomissements.
Son efficacité n'est pas établie au-delà d'un effet placebo, mais les effets indésirables cardiaques graves qu'elle peut provoquer sont connus depuis des années. Fin 2011, suite à l'examen de nouvelles données d'utilisation, l'Agence française des produits de santé (ANSM) a informé les soignants sur les troubles cardiaques graves de la dompéridone : « augmentation du risque d'arythmies ventriculaires graves et de mort subite (…) ». Début 2013, une réévaluation européenne de la balance bénéfices-risques de la dompéridone a été initiée à la demande de la Belgique. La dompéridone est aussi parfois utilisée, hors indications officielles, pour stimuler la lactation lors de l'allaitement.
En attendant, mieux vaut éviter ce neuroleptique plus dangereux qu'utile. Liste des 400 MEDICAMENTS CANCERIGENES, DONT LA BIAFINE ET LE RHINATHIOL ? Primpéran® : de moins en moins d’indications - Education du patient - médicaments. Contre les nausées, d’abord des mesures hygiéno-diététiques ©Phovoir Les indications du métoclopramide, plus connu sous son nom commercial de Primpéran®, se réduisent encore.
L’Agence européenne du médicament (EMA) recommande en effet de restreindre les prescriptions, le dosage et la durée d’administration de cet antiémitique. En raison d’un risque d’effets secondaires neurologiques graves. A la demande de l’Agence national de Sécurité du Médicament et des Produits de Santé (ANSM), le Comité des médicaments à usage humain (CHMP) de l’EMA a réévalué le rapport bénéfice/risque du métoclopramide. Rappelons à cet effet qu’en février 2012, l’ANSM avait contre-indiqué son utilisation chez les moins de 18 ans. La réévaluation des données de sécurité a confirmé le profil de risque neurologique de cette spécialité. 200.000 morts par an en Europe par les médicaments ! Les médecins français mal informés sur les médicaments et leurs effets secondaires.
Vendredi 7 juin 5 07 /06 /Juin 11:16 « une étude vient de nouveau pointer du doigt un conflit d'intérêts entre médecins et industrie pharmaceutique », et « révèle les lacunes dans le circuit d'information sur les effets secondaires graves des médicaments ». « de mai 2009 à juin 2010, l'équipe de Barbara Mintzes, de l'université de Colombie Britannique de Vancouver, a mené une étude internationale auprès de généralistes pour voir si la manière dont est réglementée l'activité des visiteurs médicaux influence la qualité du message délivré par le praticien ». « quand des visiteurs médicaux viennent informer les médecins sur les médicaments, ils omettent 1 fois sur 3 de parler des effets indésirables, et plus de 9 fois sur 10 ne parlent pas des plus graves ».

Le quotidien rappelle qu’« en France, une charte réglemente la visite médicale depuis 2005 ». Partager l'article ! InShare.