

The Deadliest Being on Planet Earth – The Bacteriophage. C'est pas sorcier -NOUVELLES THERAPIES : L'espoir est dans la cellule. AFM 60 ans de recherche. Comprendre la thérapie génique. De nouvelles stratégies contre la mucoviscidose. En France, la mucoviscidose touche environ 150 nouveau-nés par an.
Si des progrès notables ont été faits dans le traitement des symptômes, la recherche s’attaque désormais aux causes de cette maladie mortelle. «CNRS Le journal» passe en revue ces nouvelles et prometteuses stratégies thérapeutiques. Avec 7 000 personnes atteintes en France1, la mucoviscidose est la plus fréquente des maladies rares. Cette maladie génétique d’évolution progressive se manifeste souvent tôt dans l’enfance, voire dès la naissance. Parmi les symptômes potentiellement graves : des atteintes respiratoires (infection et inflammation pulmonaires) et digestives (destruction progressive du pancréas). Une meilleure espérance de vie. Thérapie génique : la micro-dystrophine restaure la force musculaire dans la myopathie de Duchenne. La myopathie de Duchenne est une maladie génétique rare évolutive qui touche de l’ensemble des muscles de l’organisme et qui concerne 1 garçon sur 3500.
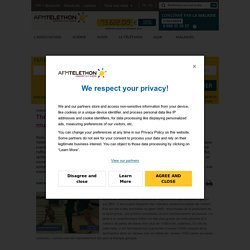
C’est la plus fréquente des maladies neuromusculaires de l’enfant. Elle est liée à des anomalies du gène DMD, responsable de la production de la dystrophine, une protéine essentielle au bon fonctionnement du muscle. Ce gène a la caractéristique d’être l’un des plus grands de notre génome (2.3 millions de paires de bases dont plus de 11000 sont codantes). Du fait de cette taille, il est techniquement impossible d’insérer l’ADN complet de la dystrophine dans un vecteur viral (ni même les seules 11000 paires de bases codantes), comme cela est habituellement fait pour la thérapie génique.
CRISPR Cas9, jouer avec l'ADN - In Cellulo #1. CRISPR-Cas9, des ciseaux génétiques révolutionnaires. CRISPR-Cas9 ("Mr. Sandman" Parody) CRISPR-Cas, une technique révolutionnaire pour modifier le génome. Jennifer Doudna Crédit photo cc by--sa YourekaScience Mise à jour 7 octobre 2020 par la rédaction Emmanuelle Charpentier et Jennifer Doudna ont obtenu le prix nobel de chimie 2020 pour leurs travaux sur le CRISPR-Cas9 Avec l’avènement du séquençage, sa rapidité et son coût de plus en plus faible, les patrimoines génétiques de très nombreux organismes vivants ont été décryptés.
Le génome humain n’y a pas échappé et la lecture complète de ses 3 milliards de lettres s’est achevée en 2003. Aujourd’hui, à peine une dizaine d’années plus tard, le séquençage intégral de n’importe quel ADN d’une taille comparable prend quelques heures et coûte moins d’un millier d’euros. Les applications du séquençage sont très nombreuses : mieux comprendre le fonctionnement des gènes, comparer les espèces entre elles et connaître leurs origines, détecter des variations ou des anomalies génétiques... Quand les bactéries sont douées d’immunité La puissance de l’outil commence à inquiéter. Et maintenant ? Thérapie génique vs Crispr-Cas9. How CRISPR lets you edit DNA - Andrea M. Henle. CRISPR/Cas9 - Lire au nid. Science et Vie N° 1166 – Novembre 2014 CRISPR/Cas9 La thérapie génique est une promesse faite il y a quelques années mais qui se heurtait à la difficulté de débusquer au cœur du génome d'un individu les gènes défectueux et de pratiquer une ''chirurgie réparatrice'' de l'ADN.
C'est bien le meilleur moyen de guérir enfin les maladies génétiques mais aussi certains cancers, des maladies auto-immunes ou cardio-vasculaires, affections encore impossible à soigner par la thérapie génique d'aujourd'hui. Depuis un an et demi pourtant cela semble possible et certaines réussites sont déjà enregistrées : des chercheurs ont rendu des cellules indestructibles face au sida et purent corriger les mutations en cause dans la mucoviscidose et la bêta-thalassémie, une anémie héréditaire, d'autres purent corriger la myopathie de Duchenne chez des embryons de souris atteints ou une maladie du foie chez le rat !
Tout cela grâce à un seul outil : CRISPR/Cas9. Espoir myopathie duchenne crispr genethon. Media figure1. Nouvelle méthode CRISPR corrige la dystrophie musculaire dans le tissu cardiaque - Traduction CV Français Anglais. CRISPR-Cas9 à l'assaut de la myopathie de Duchenne. La myopathie de Duchenne, ou dystrophie musculaire de Duchenne (DMD), est une maladie génétique rare.

Elle concerne environ un garçon sur 5 000. La maladie est due à des mutations sur le gène DMD, situé sur le chromosome X. Ce gène code une protéine, la dystrophine, impliquée dans le maintien de l’intégrité de la fibre musculaire au cours de la contraction. Le manque de dystrophine entraîne une dégénérescence progressive de l’ensemble des muscles, cœur et diaphragme inclus.
Quelle éthique pour les ciseaux génétiques ? En permettant de modifier l’ADN avec une facilité déconcertante, les outils d’ingénierie génomique comme CRISPR-Cas9 ouvrent la voie à des questionnements éthiques et législatifs complexes.
Un article à relire à l'occasion du prix Nobel de chimie 2020 attribué à Emmanuelle Charpentier et Jennifer Doudna. Peut-on toucher au génome humain ? La question ne cesse d’être posée depuis les années 1990 avec l’arrivée des thérapies géniques. Pourtant, elle est en passe de prendre aujourd’hui une dimension totalement nouvelle, avec l’émergence, en 2013, de l’édition génomique. Les outils TALEN1, ZFN2 et bien sûr CRISPR-Cas9 permettent de couper, à la base près, des séquences d’ADN choisies. Parmi ces trois outils d’ingénierie génomique, CRISPR est roi. La technologie Crispr Cas 9: un pas vers Gattaca? - 1 minute de sciences. Avez-vous déjà entendu parler de CRISPR-CAS 9 ?
CRISPR-CAS 9 (prononcez "caspère") est le nouveau jouet des scientifiques! Une technologie capable d’intervenir sur l’ADN ! Une innovation révolutionnaire capable de modifier le génome de nombreux types de cellules, tant chez les bactéries que chez les plantes ou chez les animaux, et ce avec une facilité déconcertante ! C’est le ciseau génétique que les généticiens attendaient ! CRISPR pour Clustered regularly interspaced short palindromic regions (acronyme anglais pour « courtes répétitions palindromiques groupées et régulièrement inter espacées ») est découvert en 1987 par Yoshizumi Ishino et son équipe de l’université d’Osaka (Japon) sur la bactérie Escherichia coli.
À l’époque, ces séquences énigmatiques suscitent peu d'intérêt. Ce n’est qu’en 2007 que le mystère se lève enfin: ces séquences répétées constitueraient rien de moins qu’un système immunitaire ancestral. Les premiers bébés génétiquement modifiés naissent en Chine ! Une équipe de chercheurs chinois de l’Université de Shenzhen devrait annoncer l’implantation d’embryons humains au génome modifié par la technologie CRISPR-Cas9.

Selon les informations du MIT Technology Review, l’annonce pourrait en être faite demain, au Deuxième Sommet International sur l’Edition du Génome Humain, à Hong Kong. De quoi s’agit-il précisément ? Lors d’une fécondation in vitro, les scientifiques affirment avoir introduit dans les embryons une protéine de synthèse grâce à la technique de CRISPR-Cas9, aussi dite des « ciseaux génétiques ». Cette protéine aurait alors modifié l’ADN des embryons bébés pour les rendre résistants au VIH, le virus responsable du Sida, alors que leur père est séropositif.
Ainsi, le généticien Hé Jiang a annoncé sur Youtube la naissance de Lulu et Nana, les premières jumelles génétiquement modifiées.