

Google Image Result for. Il modello atomico di Thompson e di Rutherford. Home ▸ Appunti ▸ Chimica ▸ Il modello atomico di Thompson e di Rutherford di Miriam Cipullo Joseph John Thomson è stato un fisico britannico che nel 1896 dimostrò, attraverso una serie di esperimenti, che i raggi catodici erano costituiti da piccole particelle cariche negativamente che egli chiamava ‘corpuscoli’.
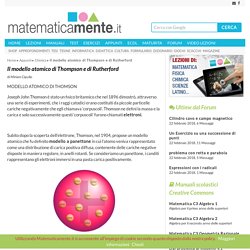
Thomson ne definì la massa e la carica e solo successivamente questi ‘corpuscoli’ furono chiamati elettroni. Subito dopo la scoperta dell’elettrone, Thomson, nel 1904, propose un modello atomico che fu definito modello a panettone in cui l’atomo veniva rappresentato come una distribuzione di carica positiva diffusa, contenente delle cariche negative disposte in maniera regolare, in anelli rotanti. Se consideriamo un panettone, i canditi rappresentano gli elettroni immersi in una pasta carica positivamente. La materia: Video - tecnologicamente. Composizione della materia _ videolezione 1. La materia - 1 Parte.
Chimica. Lezione I: Introduzione allo studio della chimica. NUMERO ATOMICO E PESO ATOMICO. Questa serie di unità audiovisive, realizzata da Rai Educational in coproduzione con l’UER (Unione Europea di Radiotelevisione), affronta i grandi argomenti delle scienze fisiche, chimiche, biologiche e matematiche con un linguaggio rigoroso e nello stesso tempo divulgativo.
Con dei grafici, disegni e animazioni questa unità illustra i concetti di numero e peso atomico. ATOMO: LA STRUTTURA ELETTRONICA. Questa serie di unità audiovisive, realizzata da Rai Educational in coproduzione con l’UER (Unione Europea di Radiotelevisione), affronta i grandi argomenti delle scienze fisiche, chimiche, biologiche e matematiche con un linguaggio rigoroso e nello stesso tempo divulgativo.
In questa unità viene spiegato con animazioni e filmati il funzionamento della struttura interna dell’atomo. Il numero atomico è dato dal numero di protoni presenti nel nucleo dell’atomo ed esprime la sua carica; esso è identico a quello degli elettroni. L’atomo è pertanto neutro, ovvero privo di carica elettrica. In ogni atomo gli elettroni si dispongono intorno al nucleo, in vari strati o livelli di energia. I gusci elettronici sono al massimo 7; il primo livello energetico, il più vicino al nucleo, può contenere al massimo 2 elettroni; il secondo e l’ultimo al massimo 8. Tags Condividi questo articolo Inserisci il codice nel tuo articolo. Perche´ si mette il sale sul ghiaccio? Laboratorio di chimica in casa/La configurazione elettronica. Wikibooks, manuali e libri di testo liberi.
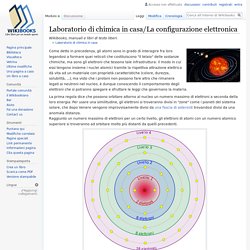
Come detto in precedenza, gli atomi sono in grado di interagire fra loro legandosi a formare quei reticoli che costituiscono "il telaio" delle sostanze chimiche, ma sono gli elettroni che tessono tale infrastruttura: il modo in cui essi tengono insieme i nuclei atomici tramite la rispettiva attrazione elettrica dà vita ad un materiale con proprietà caratteristiche (colore, durezza, solubilità, ...), ma visto che i protoni non possono fare altro che rimanere legati ai neutroni nel nucleo, è dunque conoscendo il comportamento degli elettroni che si potranno spiegare e sfruttare le leggi che governano la materia. La prima regola dice che possono orbitare attorno al nucleo un numero massimo di elettroni a seconda della loro energia.
L'immagine rappresenta i livelli che possono formarsi attorno ad un nucleo atomico. Il primo può contenere due elettroni, così gli atomi con 1 e 2 protoni avranno gli elettroni nello stesso livello. Fusione: Cos'è la Fusione ? E' la reazione nucleare che avviene nel sole e nelle altre stelle, con produzione di una enorme quantità di energia.

Come avviene ? Nella reazione di fusione nuclei di elementi leggeri, quali l'idrogeno, a temperature e pressioni elevate, fondono formando nuclei di elementi più pesanti come l' elio. Sono noti tre isotopi dell' idrogeno : l' idrogeno propriamente detto(H), il deuterio(D) e il trizio(T). I gas hanno massa (tratto da Realtà e fisica 2ed) Configurazione elettronica - L’atomo (seconda parte) Gli orbitali atomici - L’atomo (seconda parte) Atomo di Bohr e numeri quantici - L’atomo (prima parte) Modello atomico a orbitali. Chimica. La materia_Proprietà e trasformazioni fisiche: i passaggi di stato. Didattica della Chimica. Tavola Periodica degli Elementi Zanichelli. Alogeni Gli alogeni, F, Cl, Br, I, At, dal greco alos-genos, generatore di sali, sono tipici non metalli.

Creare reazioni chimiche virtuali su iPad o Tablet Android: go React. GoReact è un'app per iPad e per tablet Android progettata dal Museo della Scienza e dell'Industria di Chicago.
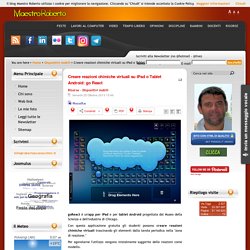
Con questa applicazione gratuita gli studenti possono creare reazioni chimiche virtuali trascinando gli elementi dalla tavola periodica nella "zona di reazione. " Per agevolarne l'utilizzo vengono inizialmente suggerite delle reazioni come modello. Sono disponibili ben 300 reazioni chimiche! GoREACT include foto e video relativi alle reazioni che gli studenti possono creare virtualmente. Vai a goREACT per iPad Vai a goREACT per tablet Android Articoli correlati. CHIMICA. Chimica.