

[40 ans] 1977 : Premier génome séquencé, la saga de l'ADN. Le génome du phage phiX174 ne comptait que 5 386 nucléotides (les constituants de l'ADN) et 11 gènes – rien à côté des génomes analysés aujourd'hui.
![[40 ans] 1977 : Premier génome séquencé, la saga de l'ADN](http://cdn.pearltrees.com/s/pic/th/premier-sequence-science-237787705)
Pourtant, le séquençage de ce virus bactérien en 1977, au prix de plusieurs mois de travail, fit sensation. Il prouvait que des outils existaient enfin pour lire l'ADN. Pour comprendre à quel point ces outils étaient attendus, il faut remonter bien plus tôt. La compréhension des mécanismes de l'hérédité ne date pas des seuls travaux, fussent-ils remarquables, du moine autrichien Gregor Mendel. Comme toute science, la génétique s'est construite pas à pas, à partir de connaissances acquises depuis des siècles par les « hybrideurs » et par la montée en puissance des méthodes statistiques. Inserm - La science pour la santé. L’édition génomique est utilisée dans différents domaines : l’agroalimentaire pour produire des espèces améliorées (par exemple des moutons et des veaux avec une masse musculaire accrue en Amérique du sud), l’agronomie (par exemple avec la modification génétique d’espèces végétales envahissantes, pour limiter leur croissance) et bien sûr la santé.
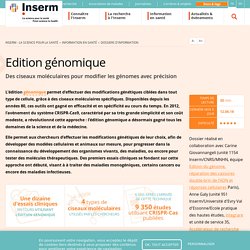
Et ce, à tous les niveaux de la recherche : fondamentale, appliquée et clinique. Toutefois, l’ensemble de ces travaux en est encore largement au stade expérimental. Produire des modèles animaux L’édition génomique permet de développer de nouveaux modèles animaux (moutons, vaches, furets, lapins, porcs, etc.), en modifiant le patrimoine génétique d’embryons grâce au système CRISPR-Cas9 avant de les transférer chez des femelles. Les chercheurs peuvent ainsi disposer à volonté de modèles animaux variés et adaptés à l’étude du développement, de pathologies ou pour des essais thérapeutiques. Produire des modèles cellulaires. Les « ciseaux moléculaires » Crispr-Cas9 distingués par le Nobel de chimie. Depuis la mise au point de la technique, en 2012, les couloirs de l’Académie suédoise des sciences bruissaient de leurs noms.
Mercredi 7 octobre, la Française Emmanuelle Charpentier et l’Américaine Jennifer Doudna ont finalement reçu le prix Nobel de chimie pour leurs travaux sur l’édition du génome et notamment la technique Crispr-Cas9. Un outil très répandu dans la recherche De façon très schématique, ces « ciseaux moléculaires » reviennent à couper un fragment d’ADN et à le remplacer par une autre séquence de son choix. Par rapport aux précédentes techniques de modification génétique, il ne s’agit plus seulement de rajouter un fragment qui viendrait se superposer à une portion défectueuse, mais véritablement de couper-remplacer le morceau choisi. Quelle éthique pour les ciseaux génétiques ? En permettant de modifier l’ADN avec une facilité déconcertante, les outils d’ingénierie génomique comme CRISPR-Cas9 ouvrent la voie à des questionnements éthiques et législatifs complexes.
Un article à relire à l'occasion du prix Nobel de chimie 2020 attribué à Emmanuelle Charpentier et Jennifer Doudna. Peut-on toucher au génome humain ? La question ne cesse d’être posée depuis les années 1990 avec l’arrivée des thérapies géniques. Pourtant, elle est en passe de prendre aujourd’hui une dimension totalement nouvelle, avec l’émergence, en 2013, de l’édition génomique. Les outils TALEN1, ZFN2 et bien sûr CRISPR-Cas9 permettent de couper, à la base près, des séquences d’ADN choisies. Parmi ces trois outils d’ingénierie génomique, CRISPR est roi. Une technique au succès fulgurant. CRISPR-Cas9: des ciseaux génétiques pour le cerveau. A l'occasion du prix Nobel de chimie attribué à Emmanuelle Charpentier et Jennifer Doudna, relisez notre article sur les ciseaux génétiques CRISPR-Cas9.
En permettant d’intervenir sur l’ADN de manière chirurgicale, ceux-ci ne font pas que révolutionner les techniques d’édition du génome, ils ouvrent aussi des opportunités enthousiasmantes pour l’étude du cerveau. Hors-série Pour la Science n°105 - novembre/décembre 2019 by Pour la Science. CRISPR peut archiver la vie d'une cellule et détecter les maladies.
CRIPSR, l’outil star de la génétique, ne sert pas qu’à modifier les gènes.
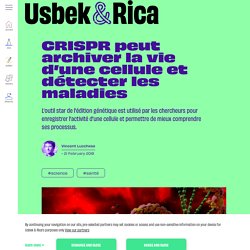
Les ciseaux moléculaires peuvent aussi transformer l’ADN en bande enregistreuse et ouvrent de nouvelles pistes pour documenter l’histoire des cellules ou détecter rapidement – et à moindre coût – les infections virales et les cancers. Trois études publiées le 15 février dernier dans la revue Science soulignent la diversité des applications potentielles promises par CRIPSR. CRISPR/CAS9 : une méthode révolutionnaire. Pourquoi Crispr révolutionne la manipulation génétique.
Crispr-Cas9 : l’édition génomique pour vaincre le cancer. Un premier test clinique se déroule aux États-Unis : l’outil d’édition génétique CRISPR-Cas 9 est utilisé pour traiter les cancers.
Les chercheurs de l’Université de Pennsylvanie à Philadelphie sont en train de tester s’il est possible de booster les cellules immunitaires des patients atteints de cancers. Ainsi, ils ont prélevé les lymphocytes T de trois patients, respectivement atteints de myélomes multiples et d’un sarcome. Avec Crisper-Cas 9, ils ont ciblé quatre gènes de ces lymphocytes T pour leur permettre de reconnaître plus efficacement les cellules tumorales. Ils ont ensuite réinjecté ces lymphocytes. Ma très chère thérapie génique. Le Téléthon 2019 a permis de récolter près de 75 millions d’euros ce week-end.
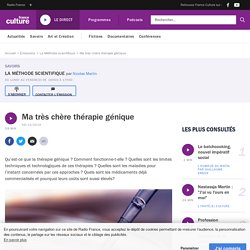
Trente-deux ans après sa création, la thérapie génique est devenue une réalité. Il y a aujourd’hui dans le monde une dizaine de médicaments en circulation, la plupart pour traiter des maladies rares, mais la thérapie génique est porteuse de nombreuses promesses notamment dans le traitement du cancer, voire pour lutter contre le VIH. Mais la route qui mène vers une généralisation de ces traitements est encore semées d’embûches, et notamment d’une de taille : celle du prix des médicaments, qui peuvent se chiffrer en centaines de milliers, voire en millions de dollars.